「21 CFR Part 11」とは、1997年に米国食品医薬品局(FDA)が施行した、電子記録(ER)と電子署名(ES)に関する連邦規則です。 一定の要件を満たした電子記録・電子署名は、紙の記録や手書き署名と同等の信頼性・法的効力を持つと認めるもので、製薬・医療機器業界のデータインテグリティ確保における世界的な基準となっています。
GxP環境下ではDXの推進に伴い文書管理の電子化が急速に進んでいますが、現場ではこんな状況が起きていないでしょうか。
「電子署名の仕組みは導入したが、署名の意味を十分に理解しないまま運用している」
「監査証跡は記録されているが、誰もレビューしていない」
こうした状態は、システムがあっても規制対応の本質を果たせていないことを意味します。
実務担当者が向き合うべきは、「21 CFR Part 11」や「ER/ES 指針」といった規制の要件を形式的に満たすことではなく、なぜその要件が存在するのかという原点を理解した上で、データインテグリティを確保する仕組みを設計することです。本記事では、「21 CFR Part 11」の基本から、電子署名・監査証跡の本質的な役割、ALCOA 原則との関係、そして実務で求められる運用設計のポイントまでを体系的に解説します。
「21 CFR Part 11」とは – FDA が定める電子記録・電子署名の規則
そもそも「21 CFR Part 11」とはどのようなものでしょうか?まずは、どこで制定された規則であり、その背景とポイントについて解説します。その上で、「21 CFR Part 11」の適用となるGxP業務と文書例を示しながら、「ER/ES指針」との関係に触れていきます。
「21 CFR Part 11」の定義と概要
「21 CFR Part 11」は、1997年に米国食品医薬品局(FDA)によって施行された、電子記録(ER)と電子署名(ES)に関する連邦規則です。CFR は「Code of Federal Regulations(連邦規則集)」の略で、21 巻(Title 21)が食品・医薬品分野、その第 11 章(Part 11)が電子記録・電子署名に関する規定にあたります。
この規則の重要なポイントは、「一定の要件を満たした電子記録や電子署名は、紙の記録や手書き署名と同等の信頼性・真正性・法的効力を持つ」と認める点にあります。製薬や医薬品の製造・開発において、ペーパーレス化を進めつつ データインテグリティ(データの完全性)を担保するための世界的な基準となっています。
なぜ厳格な要件が必要なのか - 「21 CFR Part 11」制定の背景
「21 CFR Part 11」が制定された背景には、1990 年代の製薬業界が抱えていた深刻な課題がありました。デジタル化が進む一方で、電子データは「修正痕跡を残さず改ざんしやすい」「なりすましが可能」といった脆弱性を抱えていたのです。
つまり、「21 CFR Part 11」の各要件は、こうした「改ざん」「なりすまし」「証拠の消失」といった具体的なリスクが現実に起こりうるからこそ設けられたものです。FDA は、業界のペーパーレス化を支援しつつ、人命に関わる医薬品データの信頼性を確保するため、電子システムが備えるべき厳格な管理基準を定めました。
「21 CFR Part 11」の構成(Subpart A・B・C)
「21 CFR Part 11」は次の 3 つのセクションで構成されています。
- Subpart A(一般規定):目的、適用範囲、用語の定義(クローズドシステム・オープンシステムの区別を含む)
- Subpart B(電子記録):システムが備えるべき技術的・管理的要件(バリデーション、監査証跡、アクセス制御など)
- Subpart C(電子署名):電子署名の方式や管理方法、本人確認の要件(二要素認証、生体認証など)
これらの規制を遵守することは、単なる形式的な対応ではなく、医薬品の品質と患者の安全を守るための「データの信頼性」を組織全体で保証することを意味しています。
参考:https://www.ecfr.gov/current/title-21/chapter-I/subchapter-A/part-11
「21 CFR Part 11」の対象となるGxP業務と電子文書
「21 CFR Part 11」が適用される対象は、FDA(米国食品医薬品局)の規制によって「保存や提出が義務付けられているすべての電子記録と電子署名」です。下表が示すように、製薬・医療品業界におけるGxP業務のほぼすべてが、デジタルの形で記録される限りこの規制の対象となります。これだけ広範な業務が電子化の対象となるからこそ、電子記録・電子署名の信頼性確保は、特定の部門だけの課題ではなく、組織全体で取り組むべきテーマなのです。
| 領域 | 対象業務例 | 主な電子文書例 |
|---|---|---|
| GMP | 製造工程管理 | 製造指図書、工程内検査記録書 |
| 品質保証 | 変更管理、逸脱管理、CAPA、教育訓練記録 | |
| GLP | 試験計画・実施 | 試験実施計画書、電子実験ノート |
| 報告 | 最終報告書、信頼性保証部門による監査記録 | |
| GCP | データ収集 | 電子症例報告書(eCRF)、電子患者報告アウトカム(ePRO) |
| 治験管理 | 治験実施計画書、治験薬割付記録、モニタリング報告書 | |
| GVP | 市販後調査 | 副作用症例報告書、シグナル検出記録、定期報告書 |
| GDP | 流通記録 | 配送・出荷記録、在庫管理記録、回収記録 |
ER/ES指針との関係 - 日本における電子記録・電子署名の規制
日本においても、「21 CFR Part 11」に準拠する形で2005年に厚生労働省から「ER/ES指針」(正式名称:医薬品等の承認又は許可等に係る申請等における電磁的記録及び電子署名の利用について)が発出されました。
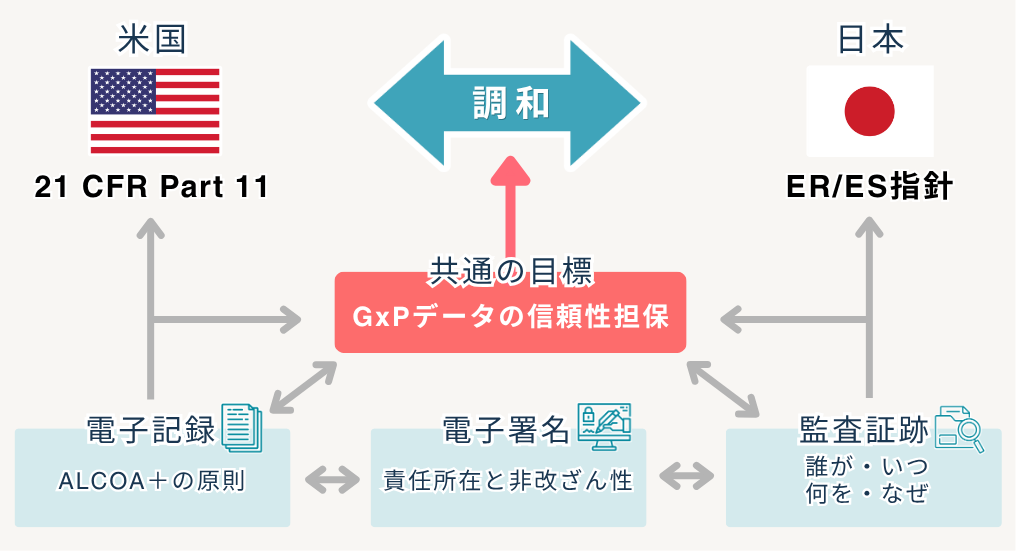
基本的な考え方はPart 11と共通しており、データの真正性・見読性・保存性の3要素を確保することが柱となっています。
- 真正性:そのデータが「本物」であり、作成者や履歴が明確で、改ざんされていないこと。
- 見読性:保存期間中、いつでも人間が「読める・理解できる」状態で表示・出力できること。
- 保存性:法定期間中、データが「失われない」ように安全に保管され続け、復元できること。
これらは、後述する ALCOA 原則(データインテグリティの国際的な基準)とも密接に関連しています。
「21 CFR Part 11」で押さえる主なポイント
「21 CFR Part 11」への対応において、実務担当者が理解すべき主要なポイントを 6 つに整理して解説します。
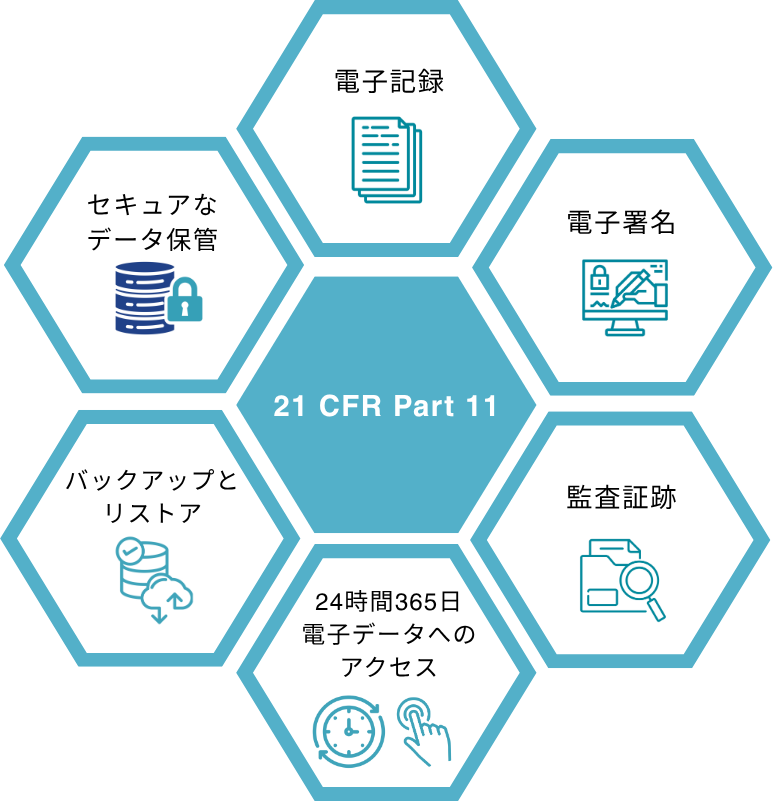
1. 電子記録 - 信頼できる形式と可読性の確保
電子記録では、信頼できる形式かつ誰でも読める状態であることが求められます。信頼できる形式として、電子記録には「いつ、誰によって、どのような条件で」生成されたデータかを示す属性情報(メタデータ)や操作履歴が含まれている必要があります。
また、これらの情報がPDFのような汎用性が高い標準的なファイル形式で出力されることが重要です。誰でも読める状態にするには、パソコンのディスプレイ上で明瞭に表示されつつ、紙に印刷した際に内容が劣化せず、誰でも読める状態を保つ必要があります。
2, 電子署名 - 手書き署名と同等の信頼性を担保する要件
電子署名について「紙への手書き署名」と同等の信頼性を持つための具体的なルールが定められています。電子署名が付与された記録には「署名者の氏名」「署名の日時」「署名の意図(作成・確認・承認)」が求められます。電子署名は「個人に固有」であり、他者への再割り当てや使い回しは厳格に禁止されています。そのため、署名権限を付与する前に、その人物が本人であることを確認しなければなりません。
また、電子署名に使用するIDやパスワードの共有は禁止されています。そして、署名の不正利用を防止するために、IDとパスワードの組み合わせによる認証の他、生体認証(バイオメトリクス)を用いる方式も重要になっています。
3. 監査証跡(Audit Trail) - データの変更履歴を自動記録する仕組み
監査証跡では、データの作成・変更・削除の履歴を記録する必要があります。具体的には「いつ、誰が、何を、なぜ」操作したかを、システムの操作者が変更・削除できないようにし、システムが自動的に記録できるようにすることが重要です。
4. アクセス制御とセキュリティ - 物理的・論理的管理の両立
システム内のデータにアクセスできるのは、あらかじめ許可された特定の個人に限定されなければなりません。 そのためには、物理的なセキュリティと論理的なセキュリティの両方からのアクセス制御・管理が必要となります。物理的なセキュリティでは、居室への入退室管理、USBメモリや外部メディアの利用制限が重要となります。論理的なセキュリティでは、個人ごとに固有のIDとパスワードの組み合わせに加え、データを「作成する人」と「承認する人」、そして「システムを管理する人」を明確に分ける職務分離の設定が重要になります。
5. 記録の保持 - データライフサイクル全体での保護
作成されたデータは、法令で定められた期間中(例:有効期限+数年)、消失や劣化から守られなければなりません。まず、保存期間を通じて、データが意図的または偶発的に変更されないよう保護する必要があります。また、作成されたデータと監査証跡のデータがセットで保持されることが必要であり、安全な媒体へ移動・保管できるようにすることが大切です。
6. バリデーション(CSV) - システムの適格性を検証する
電子記録を生成、変更、維持、保存、または取得するシステムは、その性能が意図した通りであることを証明しなければなりません。そのために行われる検証作業が「バリデーション」であり、コンピュータ化システムバリデーション(CSV:Computerized System Validation)とも呼ばれます。
バリデーションではシステムが正確で、信頼性が高く、意図した通りの性能を維持していることを一貫して実証する必要があります。これにより、データの欠落や意図しない処理エラーを未然に防ぎます。
データインテグリティとALCOA原則 | 「21 CFR Part 11」が守る本質
「21 CFR Part 11」が最終的に守ろうとしているのは、「データインテグリティ(データの完全性)」です。データインテグリティとは、データがライフサイクル全体を通じて完全で、一貫性があり、正確であることを保証する概念です。
データインテグリティを評価する国際的な基準として広く用いられているのが、ALCOA 原則(ALCOA+)です。
| 要素 | 内容 |
|---|---|
| A:Attributable(帰属性) | 誰が、いつデータを作成・変更したかが明確であること |
| L:Legible(判読性) | データが読みやすく、長期にわたって参照可能であること |
| C:Contemporaneous(同時性) | 作業が行われたその時に記録されていること |
| O:Original(原本性) | データが原本であること、または検証済みの真正コピーであること |
| A:Accurate(正確性) | データが正確で、編集や誤りがないこと |
さらに近年では、ALCOA に以下の 4 要素を加えた ALCOA+(CCEA)の遵守も求められています。
| 要素 | 内容 |
|---|---|
| C:Complete(完全性) | データが欠落なくすべて揃っていること |
| C:Consistent(一貫性) | データの日時や順序に矛盾がないこと |
| E:Enduring(耐久性) | データが長期間保存され、消失しないこと |
| A:Available(利用可能性) | 必要なときにいつでもデータにアクセスできること |
「21 CFR Part 11」の各要件(電子署名、監査証跡、アクセス制御、記録の保持、バリデーション)は、この ALCOA+ 原則を電子システム上で実現するための具体的な手段と位置づけることができます。ER/ES 指針が求める「真正性・見読性・保存性」も、ALCOA 原則の考え方と本質的に一致しています。
電子署名と監査証跡の役割 - なぜ「車の両輪」なのか
電子署名と監査証跡には、それぞれの役割と求められる機能があります。ここで重要なのは、個々の機能を知ることではなく、これらが最終的に何を実現するためのものかを理解することです。電子署名と監査証跡が果たすべき最終目標は、「電子記録の証拠能力の証明」すなわちデータインテグリティの担保にあります。この目標を念頭に置いた上で、それぞれの役割と機能を見ていきましょう。
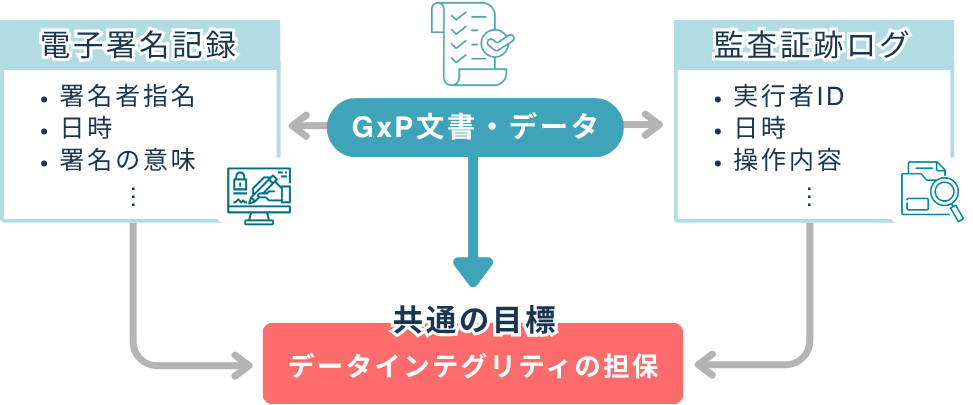
電子署名の役割と求められる機能
電子署名には、従来の紙と印影による署名と同等、あるいはそれ以上の信頼性を担保する役割があります。具体的には、署名者が間違いなく本人であることを、IDとパスワードを用いて特定する役割があります。また、署名が個人に固有であり、他人に譲渡できない仕組みによって守る役割があります。
21 CFR Part 11(Subpart C)や国内のER/ES指針において、システムには次の機能が備わっていることが求められます。
- 署名に付随する情報として「署名者の氏名」「署名の日時(正確なタイムスタンプ)」「署名の意図(作成・確認・承認)」を記録する。
- 認証方式としてIDとパスワードのように、2種類以上の要素を用いて認証する(二要素認証)。
- 署名は、対象となる電子記録から切り離して他の文書に使い回すことができないようにする。
監査証跡の役割と求められる機能
監査証跡では、「どのような操作を経て最終結果に至ったか」を再現できることが望まれます。そのためには、改ざん防止のため「すべての操作が記録されている」ことが、意図的な書き換えやデータ削除に対する抑止力となります。また、コンプライアンスや内部統制の観点で正しく作業が行われたことを客観的に示す役割があります。
しっかりした監査証跡を残すため、システムには次の機能が備わっていることが求められます。まず、以下の要素が、システムによって自動的に記録される必要があります。
- Who(誰が):操作した個人のユーザーID
- When(いつ):正確な日時(タイムスタンプ)
- Why(なぜ):データ記録時の理由
また、すべての操作の記録が残されている必要があるため、データを変更した場合、その変更前と変更後の記録を残す機能が必要となります。尚、監査証跡を記録する設定はシステム利用者によって「オフ」にされたり、内容を「編集・削除」されたりすることがあってはなりません。
電子署名と監査証跡が「車の両輪」である理由
「電子署名」と「監査証跡」の機能は、車の両輪のような関係にあり、一方が欠けても成立しません。
- 電子署名は「誰が(帰属性)」と「承認の意志」を証明します。
- 監査証跡は「いつ、どのように(同時性・正確性)」データが作られたか、その経過を証明します。
もし一方が欠けると次のことが起きてしまいます。
- 電子署名のみの場合
「結果」は承認されていますが、その結果に至るまでにデータが何回修正や変更されてきたのか、あるいは1回で正しく導きだされたものかという「過程」が見えなくなります。 - 監査証跡のみの場合
結果に至るまでの「過程」はすべて残っていますが、「誰が」その最終結果に責任を持って「承認」を出したのかという「責任の所在」が不明確になります。
このように、データは作成されてから保存期間が終了するまでの間、改ざんされてしまうリスクが潜んでいます。そのリスクを軽減するために、電子署名により、署名をした瞬間にデータはロックされ、原則変更できなくします。そして、監査証跡により、署名後にデータを修正した場合でも、その変更事実が監査証跡に「署名後の修正」としてしっかり記録されます。設計段階から、電子署名と監査証跡を必ずセットで考えることが重要です。
21 CFR Part 11対応の実務 - 規制対応と業務効率化を両立する仕組みづくり
法規制に対応しながら、GxP環境下での業務を効率化することは大変な労力が必要になります。やみくもにシステムを入れただけでは業務は上手く回りません。ここでは、実務の運用を考えた仕組み作りの重要性やポイントと、その一助となる「GMOサイン証跡管理DX」の活用ポイントを紹介します。
「システム導入=完了」ではない - 運用設計が成否を分ける
21 CFR Part 11に対応しながら、GxP環境下での業務において文書管理の電子化・電子署名・監査証跡の取得を進める上で、多くの企業が直面する落とし穴は「高機能なシステムを導入すれば終わり」と考えてしまうことです。しかし、システムは単なる道具に過ぎません。重要なことは、医薬品や医療機器の品質と患者様の安全を守るための「データの信頼性」を組織全体で保証することです。
そのため、システムそのものではなく、それを「人間がどのように正しく運用し、信頼性を維持し続けているか」という運用上の仕組みが重要となります。どんなに優れた監査証跡機能があっても、誰もそれをレビューしていなければ改ざんや誤操作を放置している、つまりリスクを見逃して業務を運用し続けることになります。
視点 1:教育訓練の徹底と品質文化の醸成
最初に強調すべきは「人」の問題です。どれだけ良い仕組みを設けたり、法規制対応に向けた対策を行っても、最後にこれらを業務で運用するのは人間です。普段業務で使用するデータや文書に対して「手順だから守れ」というスタンスではなく、電子署名・監査証跡がなぜ重要なのかを社員が理解する「品質文化」を醸成することが、すべての出発点となります。特に、GxP 環境下でのデータや文書の意図的な改ざんや、無知による誤操作が会社の信頼を失墜させるリスクがあることを共有することが大切です。
視点 2:証拠の残し方 | いつでも遡れる仕組みをつくる
人の理解を土台とした上で、客観的な証拠や証跡を確実に残す仕組みが必要です。電子署名であれば、いつ誰が署名したものか、その履歴が追える仕組みが必要になります。また、監査証跡についてはその記録が自動的にすべて保管され、いつでもレビューできる状態にしておく必要があります。これにより、データや文書の真正性が確保され、いつでも再確認できるようになります。
視点 3:技術的セキュリティと管理的セキュリティの両立
技術的対策(システム)と、管理的対策(SOP・規程)で守る部分を明確に分けます。具体的には、「パスワードの共有禁止」はSOP(標準手順書)で規定しつつ、システム側では管理者より「ユーザーとアクセス制御」を設定します。これにより、両者が噛み合って初めて有効なセキュリティとなります。
視点 4:データライフサイクル全体の設計
データの作成、解析、報告だけでなく、バックアップ、アーカイブ、そして最終的な破棄までを一つの流れとして設計します。特に、GxP環境下のデータ・文書・監査証跡は「有効期間+数年」保持しなければなりません。また、これらのデータはすぐに取り出せる状態にしなければならないため、通常の保管先とセキュアなバックアップ先の選定、リストアテストした時にデータを読める状態(生データの他にPDF化するなど)にする仕組みが必要になります。
GMOサイン証跡管理DXの活用 - 21 CFR Part 11対応を支援するツール
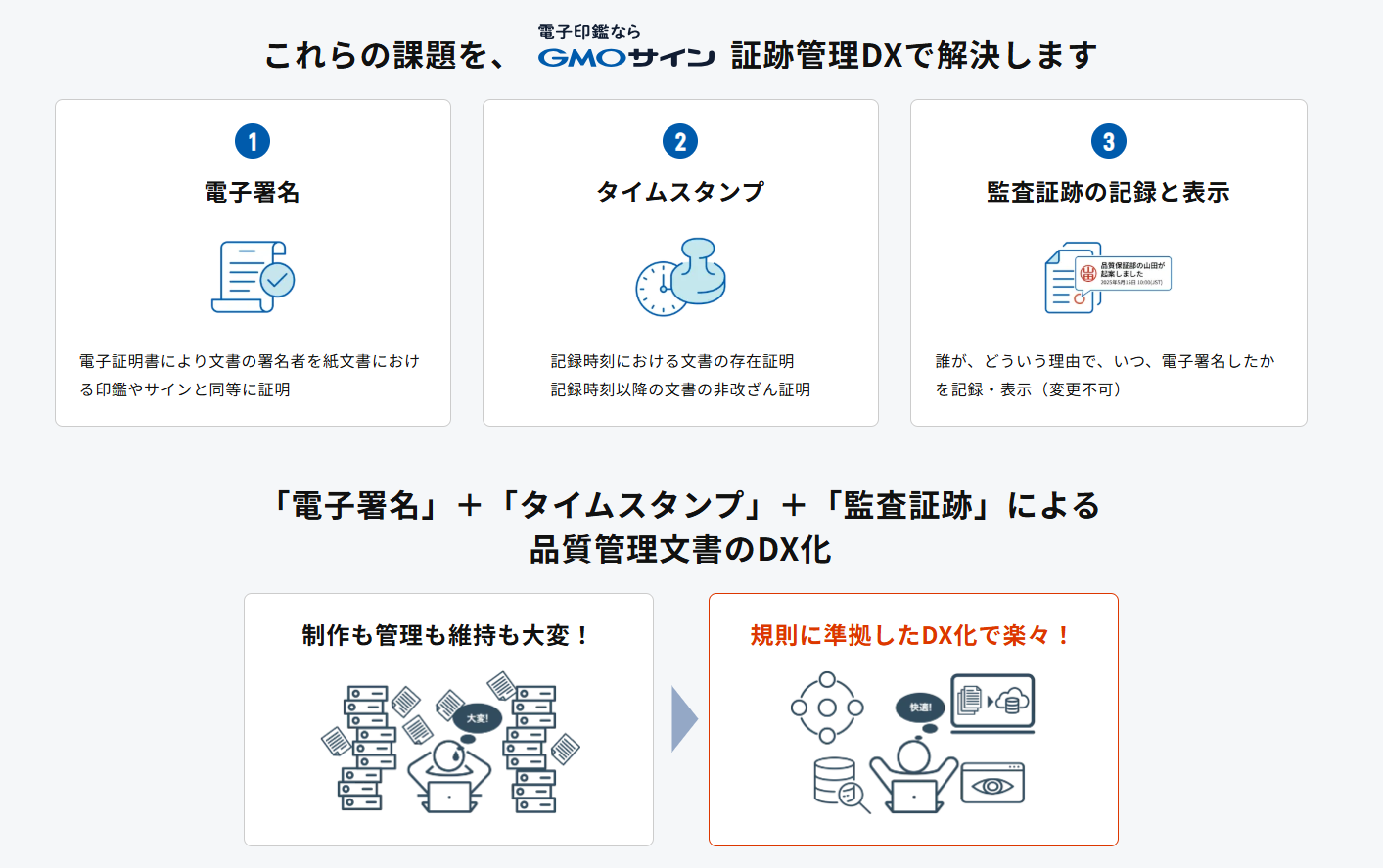
前述の運用設計を踏まえた上で、それを支えるツールとしてどのように「GMOサイン証跡管理DX」を有効活用できるか見ていきましょう。「GMOサイン証跡管理DX」は、上記の運用設計の各視点に対応する形で、以下の機能を備えています。
視点1「教育訓練と品質文化」への対応
「GMOサイン証跡管理DX」はコンピュータ化システムとしてバリデーション済みであり、ご契約のお客様に無償でバリデーション報告書を提供可能です。これにより、教育訓練で使用するシステムそのものの適格性を証明する手間を削減し、担当者が「なぜこのシステムを使うのか」を理解した上で運用に入ることができます。
視点2「証拠の残し方」への対応
文書(データ)の各署名時に「誰が・いつ・どういった理由で」署名したかが監査証跡として自動記録・表示・保管されます。署名ごとにタイムスタンプと電子証明書が付加されるため、署名の同時性と帰属性が確保されます。また、署名途中・完成した文書の変更はできない仕組みとなっており、改ざん防止が担保されます。
視点3「技術的・管理的セキュリティの両立」への対応
メールアドレス・パスワードおよびパスコードによる二要素認証に加え、管理者によるユーザーのアクセス制御・権限設定が可能です。SOPで「パスワード共有禁止」を規定しつつ、システム側で強制的にアクセス制御を行うという、管理と技術の両立を支援します。
視点4「データライフサイクル全体の設計」への対応
署名済み文書はクラウド上に容量上限なく長期保管され、随時閲覧とダウンロード(複製)が可能です。PDFでの保管・出力にも対応しているため、将来のシステム移行時にもデータの見読性を維持できます。
このように、「GMOサイン証跡管理DX」は法規制に対応しつつ、GxP環境下における電子署名・監査証跡の実務運用に要素に対応しており、現業務に当てはめることができます。これにより業務を運用しながら、文書の電子化や業務効率化の一助となります。
▼FDA「21 CFR Part 11」など国際規則要件にも対応!詳細はこちら
GMOサイン 証跡管理DX 特設ページを見る
まとめ :「21 CFR Part 11」対応を「データの信頼性を軸にした変革」へ
「21 CFR Part 11」への対応は、単なる規制遵守ではなく、企業の透明性と信頼性を築くデータインテグリティの要です。電子化はあくまで手段であり、本質は監査証跡による徹底した記録と、実務に即した適切な運用設計にあります。
要件整理や業務運用の見直しに「GMOサイン証跡管理DX」のような支援ツールを上手く取り入れ、規制対応と業務効率化を両立した品質管理体制の構築を目指していきましょう。


























